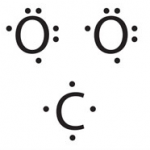
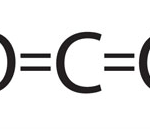A continuació tens la representació gràfica de quatre reaccions químiques. Aquestes representacions s’anomenen equacions químiques. Observa-les amb detall i reflexiona sobre els conceptes que et plantegem més avall:
Els símbols dels elements – ANOTA
Ja us haureu adonat que els químics treballen amb un llenguatge especial. És necessari que el comencis a conèixer. Per això et demanem que busquis quin és el símbol dels següents elements químics i que ens diguis alguna característica de cada un (per a què es poden utilitzar, on es troben…).
Elements i compostos – ANOTA
En les equacions químiques, les diferents substàncies es representen amb una fórmula anomenada fórmula química. Fixa’t bé amb les fórmules que apareixen en les reaccions de l’entrada anterior (les hem tornat a reproduir) i intenta classificar-les en dos grups.
Les substàncies que t’han quedat en un dels grups s’anomenen elements i les de l’altre grup compostos. En què es diferencien ? tens cinc minuts per pensar-ho abans que ho expliqui el professor.
I ara practica… ajustant reaccions – ANOTA
Un cop coneixes el concepte de reacció química, hauries de tenir clar que la matèria, no es crea ni es destrueix, sinó que es transforma. Això és el que anomenem el principi de conservació de la matèria. Tenint en compte això, posa’t a prova. En aquest enllaç hi trobaràs una sèrie de reaccions que necessiten ser ajustades. Som-hi!
Per acabar de practicar una mica aquí tens unes quantes equacions quimiques per ajustar.
Molècules i àtoms – OBSERVA
Reactius i productes – ANOTA
Us heu fixat que totes les reaccions que heu anat veient tenen una fletxa? Aquesta ens indica que hi ha hagut un canvi químic. Però què és un canvi químic?
Un cop fet això, hauràs deduït que existeixen uns tipus de canvis que n’anomenem químics i uns altres que en diem físics. Observa els canvis que trobaràs aquí i classifica’ls segons de quin tipus siguin. Explica el perquè a la teva llibreta.
Les reaccions i l’energia -OBSERVA
Sempre que els reactius es transformen en els productes es produeix un intercanvi d’energia amb l’entorn. A vegades, perquè pugui tenir lloc la reacció, cal afegir energia. Aquesta energia s’agafa de l’entorn i entra a la reacció. Es tracta de les reaccions ENDOTÈRMIQUES.
Sabries posar algun exemple de reacció exotèrmica ?
Per què existeix un sistema de coordinació diferent del nerviós ? – LLEGEIX I ANOTA
El sistema nerviós és el principal encarregat de fer aquesta funció però no és l’únic. L’aparell endocrí també realitza part d’aquesta tasca.
El sistema nerviós està especialitzat en donar respostes ràpides. Rep un estímul ja sigui procedent de l’exterior (per mitjà dels òrgans dels sentits) o bé de l’interior (per mitjà de sensors interns) i elabora una resposta que executa immediatament.
Hi ha d’altres respostes que ha de donar el cos que no són tant ràpides i que no s’han de produir en un instant concret. És més, a vegades són respostes que s’han d’allargar en el temps. Aquest tipus de respostes no les pot donar el sistema nerviós. Ho fa l’aparell endocrí.
El creixement dels ossos, la maduració dels òrgans sexuals, el metabolisme general del cos, el creixement del pèl, el desenvolupament de la musculatura, el canvi de la veu… Tots aquestes exemples són processos lents i que necessiten temps per produir-se. Els estímuls ràpids i instantanis dels impulsos elèctrics que el sistema nerviós dóna no ens serien útils.
L’aparell endocrí no genera impulsos elèctrics de ràpida transmissió a través dels nervis sinó que genera unes substàncies químiques (unes molècules) anomenades hormones i que es tranporten pels vasos sanguinis fins al seu destí.
Des de que una hormona és sintetitzada fins que arriba a l’òrgan on ha de fer efecte poden passar hores i a més pot fer la seva funció en aquell òrgan durant un temps perllongat.
Així com els impulsos elèctrics deixen de fer el seu efecte de manera instàntània, les hormones han de ser degradades pels teixits perquè cessin el seu efecte.
L’estructura de l’àtom – ESCRIU
Escriu un text en el que apareguin correctament contextualitzats els següents conceptes: electró, àtom, nucli, protó, escorça, neutró.
A continuació en llegirem alguns.
Una mica de teoria sobre les reaccions – TEORIA
Glàndules exocrines i endocrines – INVESTIGA
I encara una mica més… – TEORIA
Experiment de Thomson
L’experiment de Rutherford – LLEGEIX I INVESTIGA
El model de Rutherford – LLEGEIX i INVESTIGA
Per fer sostenible el seu model Rutherford no va tenir més remei que buscar la manera perquè els electrons no caiguessin sobre els protons i l’àtom tornés a ser massís la solució va ser que els electrons havien de girar.
1. Per què penses que això va ser una solució ?
En segon lloc calia trobar una manera perquè els protons no es rebutgessin ja que si se separaven tampoc s’haguessin explicat els resultats de l’experiment de la làmina d’or. La manera va ser suposar que hi havia unes partícules sense càrrega que es disposaven entremig dels protons.
2. Per què els neutrons van suposar una solució al segon problema ?
Les dimensions de l’àtom – LLEGEIX
Però, a desgrat d’aquesta enorme quantitat d’elements que hi ha a l’ interior d’una partícula de matèria, aquests elements són tan infinitament minúsculs i estan tan separats que entre les partícules elementals hi ha un buit inmens. Avui que qualsevol cosa diuen que al·lucina, proposo al lector barceloní aquests joc d’ imaginació: que clavi una agulla en un coixí del seu sofà. Si el cap d’ aquesta agulla representés el protó d’un nucli d’oxígen, l’electró que gira al seu voltant seguiria una circumferència que passaria per Portugal,França,Itàlia i Algèria.
Entre Barcelona i París ,per dir-ho així,res.Les partícules que constitueixen una clau de ferro,el tronc d’ un arbre, el d’ un gos es mouen en un enorme desert buit.J.M.Espinàs,Avui(14 set.1991)”
Els models atòmics – AUTOQÜESTIONARI
Respon el següent autoqüestionari sobre els models atòmics per repassar.
La necessitat d’ordenar – PENSA
Pensa possibles maneres d’ordenar-los i anota-les als apunts. Tot seguit les posarem en comú i triarem les que ens semblin millor.
La taula periòdica – OBSERVA
Ja has vist que molts dels mètodes que heu proposat per a la classificació dels elements químics no són massa vàlids. El 1869, el senyor de la fotografia va proposar un sistema de classificació que es coneix com a Taula Periòdica dels Elements i que corregida és la que avui encara s’utilitza. Et demanem ara que en consultis una i esbrinis per quina característica están ordenats els àtoms. Si ets observador en trobaràs una, si ho ets encara més en trobaràs dues, i si ho ets molt veuràs que només una de les dues és vàlida.

Tornem a la taula periòdica
Aturem-nos-hi un moment – TEORIA
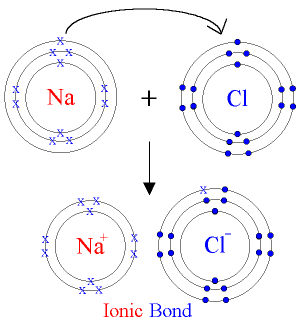
Els ions
Fins ara hem vist l’estructura interna d’un àtom i sabràs que el balanç entre les càrregues elèctriques entre els electrons (negativa), protons (positiva) i neutrons (neutra) és zero. Per tant, les càrregues elèctriques d’un àtom estan compensades.
Pensa però, si aquesta estructura pot variar en funció de la pèrdua o de la incorporació d’alguna d’aquestes partícules. Fixa’t en la imatge següent i busca el nom dels àtoms o les molècules que sofreixen aquestes modificacions:
The elements song by Theodore Gray
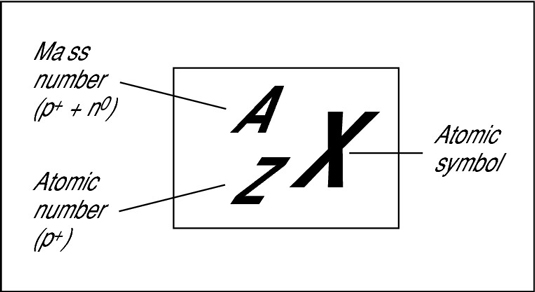
Nombre atòmic i nombre màssic-OBSERVA I ANOTA
Observa atentament aquestes imatges. Què en dedueixes? Pensa-hi una estoneta i en parlem a classe.
Per practicar pots fer els següents exercicis online.
Ara fes els exercicis següents a la teva llibreta.
A la recerca de les glàndules endocrines – POU
Fes una recerca per la xarxa i troba una imatge de cada una de les glàndules endocrines del cos. Et suggerim que facis una taula de qautre columnes on a la primera posis el nom de la glàndula, a la segona la localització, a la tercera el nom d’alguna de les hormones que fabrica i finalment a la quarta, la imatge de la glàndula.
Una vegada enllestit ho penges al pou anomenat: Glàndules endocrines”.
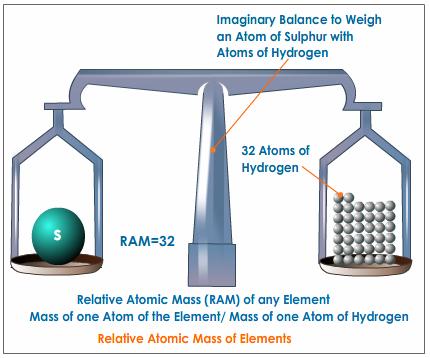
Les unitats de massa atòmica – PENSA
La massa atòmica – INVESTIGA
Ja has vist que els àtoms estan formats per tres partícules bàsiques. Hem parlat de la càrrega elèctrica d’aquestes partícules però ara és el moment de dir alguna cosa sobre la seva massa.
Pesa un àtom ? Què en penses ?
Si la resposta és afirmativa i l’àtom només està format per electrons, neutrons i protons quina conclusió en treus ? és a dir què és el que fa que l’àtom pesi ?
T’avancem que una de les tres partícules no influeix en la massa de l’àtom. Amb un minut i abans de continuar llegint, busca quina és aquesta partícula i busca si les altres dues pesen i quant pesen. Anota-ho al diari.
Clica aquesta taula periòdica i busca a veure si ens dóna informació sobre el número màssic. El trobes ? Mira-ho bé. Hi és o no ?
Ara clica de nou la mateixa taula periòdica d’abans i busca si hi ha la massa atòmica ? Hi és ? Si hi és busca els àtoms d’hidrogen, de carboni, d’oxigen i de ferro anota’n la seva massa atòmica al diari de classe.
Què et sorprèn d’aquestes masses ?
Intenta trobar-hi una explicació. Si vols una pista clica aquí. Hi trobaràs una taula anomenada “Taula dels isòtops”.
A veure si te’n surts !
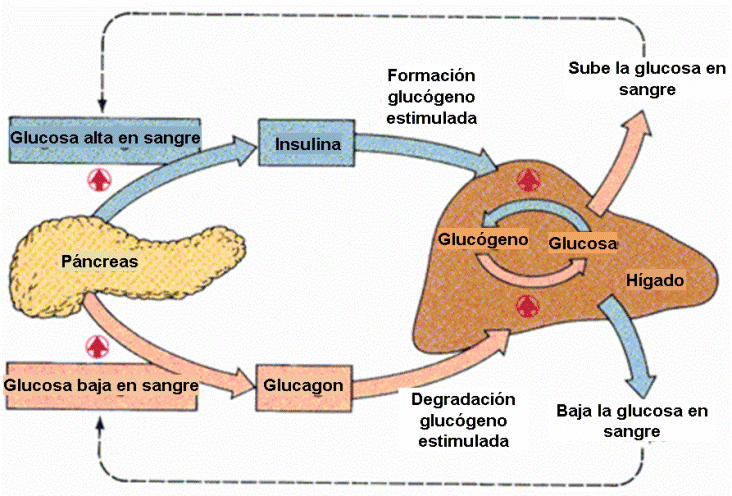
El sistema insulina-glucagó
Llegim-ho a poc a poc – TEORIA
L’aparell endocrí és jeràrquic – INVESTIGA
Atenció que aquesta activitat és de nivell !
A continuació tens una imatge (la pots clicar per fer-la més gran) que il·lustra el funcionament jeràrquic de l’aparell endocrí.
OBSERVA AMB ATENCIÓ EL DIBUIX I RESPON LES PREGUNTES EN EL TEU DIARI

1. On està situat l’hipotàlem ? quina creus que és la funció de l’hipotàlem ? què t’ho fa pensar ?
2.La hipòfisi està dividia en dues parts anomenades adenohipòfisi i neurohipòfisi. Tant l’una com l’altra segreguen hormones però quina diferència hi ha entre les hormones que fabrica una i altra part ? (Pista: la diferència no està tant en les hormones com en el seu recorregut).
3. Pel que fa a les hormones fabricades per l’adenohipòfisi, l’ACTH, la TSH, la FSH tenen una diferència important amb la GH i la LTH. Pensa quina pot ser.
Càlcul de la massa molecular – PRACTICA
L’aparell endocrí – TEORIA
Configuració electrònica – INVESTIGA
Si els àtoms només estiguessin ordenats segons el numero atòmic, perquè l’hidrogen i l’heli estan tant lluny l’un de l’altre ? o en canvi el sodi i el magnesi estan tant a prop ?
La solució es troba en les electrons. Observa bé aquestes imatges i treu-ne coclusions. Seria bo que en una pantalla a part tinguessis oberta una taula periòdica.
Ah sí ! Sàpigues que aquestes imatges fan referència a la configuració electrònica que veureu a fons a 4t d’ESO.
Si no n’has acabat de treure l’aigua clara et deixem aquí aquest document que de ben segur t’ajudaràs. Som-hi !
Estabilitat i reactivitat – INVESTIGA
Repassem-ho una mica – TEORIA
L’enllaç iònic – INVESTIGA
Enllaç covalent – OBSERVA I ANOTA
En l’enllaç iònic, els àtoms s’uneixen mitjançant la pèrdua d’electrons de l’últim nivell i el guany d’aquests per part de l’altre àtom. D’aquesta manera, els elements dels grups I , II i III s’uneixen amb facilitat amb els elements dels grups XV, XVI i XVI.
No obstant, existeix una altre mètode per unir-se: la compartició dels electrons. Fixa’t en la imatge següent:
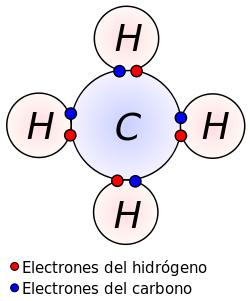
La molècula de metà (CH4) s’uneix mitjançant l’enllaç covalent. Aquest consisteix en compartir els electrons de l’última capa de valència entre els àtoms que formen la molècula. En el cas del carboni (que té 4 electrons a l’última capa), pretén aconseguir-ne 4 més per assolir la estabilitat màxima (completar el nombre màxim d’electrons a l’última capa, és a dir, 8). Per fer-ho, els “agafa” de 4 hidrògens. De la mateixa manera, l’Hidrogen pretén assolir una estabilitat major omplint el seu primer i únic nivell (al qual hi caben dos electrons i prou). Cada hidrogen doncs, “agafa” un dels electrons del Carboni per assolir l’estabilitat màxima.
D’aquesta manera s’uneixen la majoria de biomolècules orgàniques, com l’aigua (H2O) i la glucosa (C6H12O6) , així com d’altres molt més complexes.
Mira’t el vídeo següent i distingeix els dos enllaços que hem vist fins ara. Sabries esquematitzar la unió dels àtoms de C i O per formar el diòxid de carboni? Fes-ho a la llibreta.
Representació de Lewis – INVESTIGA
Existeix una manera molt interessant per entender i representar els enllaços covalents. S’anomena representación de Lewis i tot seguit t’adjuntem tres imatges d’aquesta representació. Estan ordenades cronològicament. És a dir la primera és abans de que els àtoms s’uneixin i la darrera és un cop están units.
Series capaç de descobrir com funciona aquesta representació ? i sobretot copsar la seva utilitat ?
Algunes representacions – PRACTICA
Ara que ja saps com es representen els enllaços covalents, almenys sobre el paper, seria qüestió de fer una mica de pràctica. Algunes són molt fàcils però d’altres es compliquen molt. A veure com se’t dóna…
Et proposem que representis les següents molècules que s’uneixen per mitjà d’un enllaç covalent.
N2; NH3; C2H6; C4H10; CH4O; CCl4; C2H6O
Enllaç covalent – VIDEOS
A continuació tens dos vídeos sobre enllaços covalents. Fes-hi un cop d’ull.
oxygen_double_bond (Enllaç covalent de la molècula d’oxigen).
covalent_bond_water (Enllaç covalent de la molècula d’aigua).
Repassem els enllaços – OBSERVA I ANOTA
Fins ara hem començat a veure quines característiques presenta l’enllaç iònic i el procediment pel qual es duu a terme. Recordes quins altres dos tipus d’enllaços hi ha? Com s’anomenen?

Mira’t la següent presentació i consolida el que saps sobre l’enllaç iònic. a més a més, comença a buscar les diferències entre els dos altres tipus d’enllaç.
Després el professor farà una explicació amb apunts que hauràs de tenir ben organitzats al diari de classe. Som-hi!
Enllaç metàl·lic – INVESTIGA
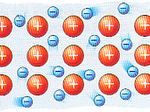
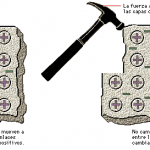
Llegeix el següent text que defineix l’enllaç metàl·lic. Destaca’n les paraules importants i intenta fer-te una idea del què és aquest tipus d’enllaç:
L’enllaç metàl·lic és característic dels elements metàl·lics, és un enllaç fort, primari, que es forma entre elements de la mateixa espècie. Els àtoms, a l’estar tan propers l’un de l’altre, interaccionen els nuclis juntament amb els seus núvols electrònics empaquetant-se en les tres dimensions, pel que queden envoltats de tals núvols. Aquests electrons lliures són els responsables que els metalls presentin una elevada conductivitat elèctrica i tèrmica, ja que aquests es poden moure amb facilitat si es posen en contacte amb una font elèctrica. Presenten lluentor i són mal·leables.
Els elements amb un enllaç metàl·lic estan compartint un gran nombre d’electrons de valència, formant un mar d’electrons envoltant un enreixat gegant de cations.
Tot seguit tens unes imatges que et poden ajudar:
Vacunem o no vacunem ?
Darrerament hi ha la “moda” de no vacunar. Això porta molts problemes. Aquesta entrevista ens pot aclarir els dubtes !
Mètodes de separació – INVESTIGA
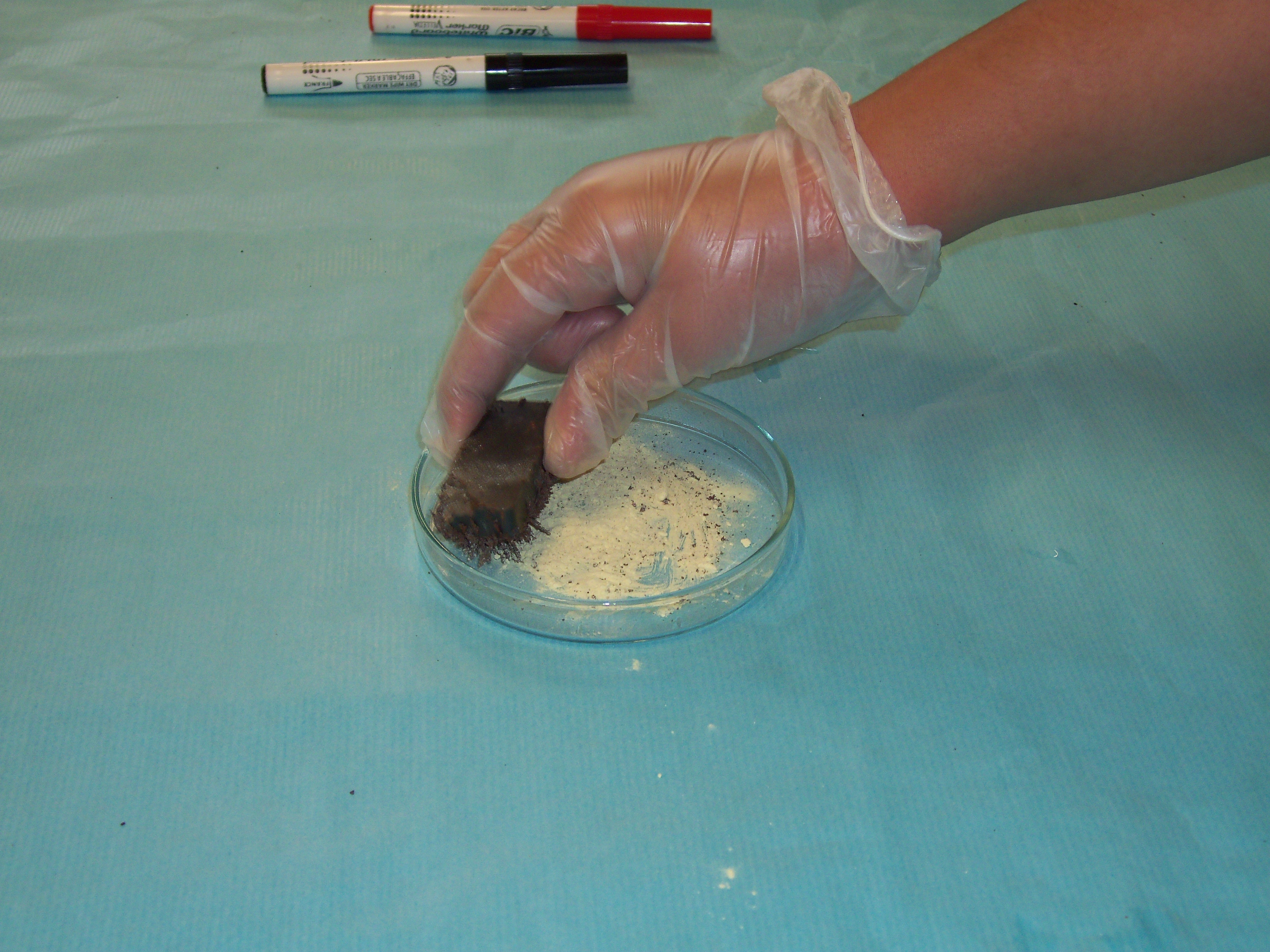
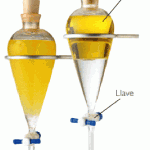
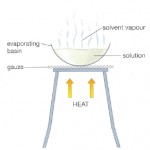
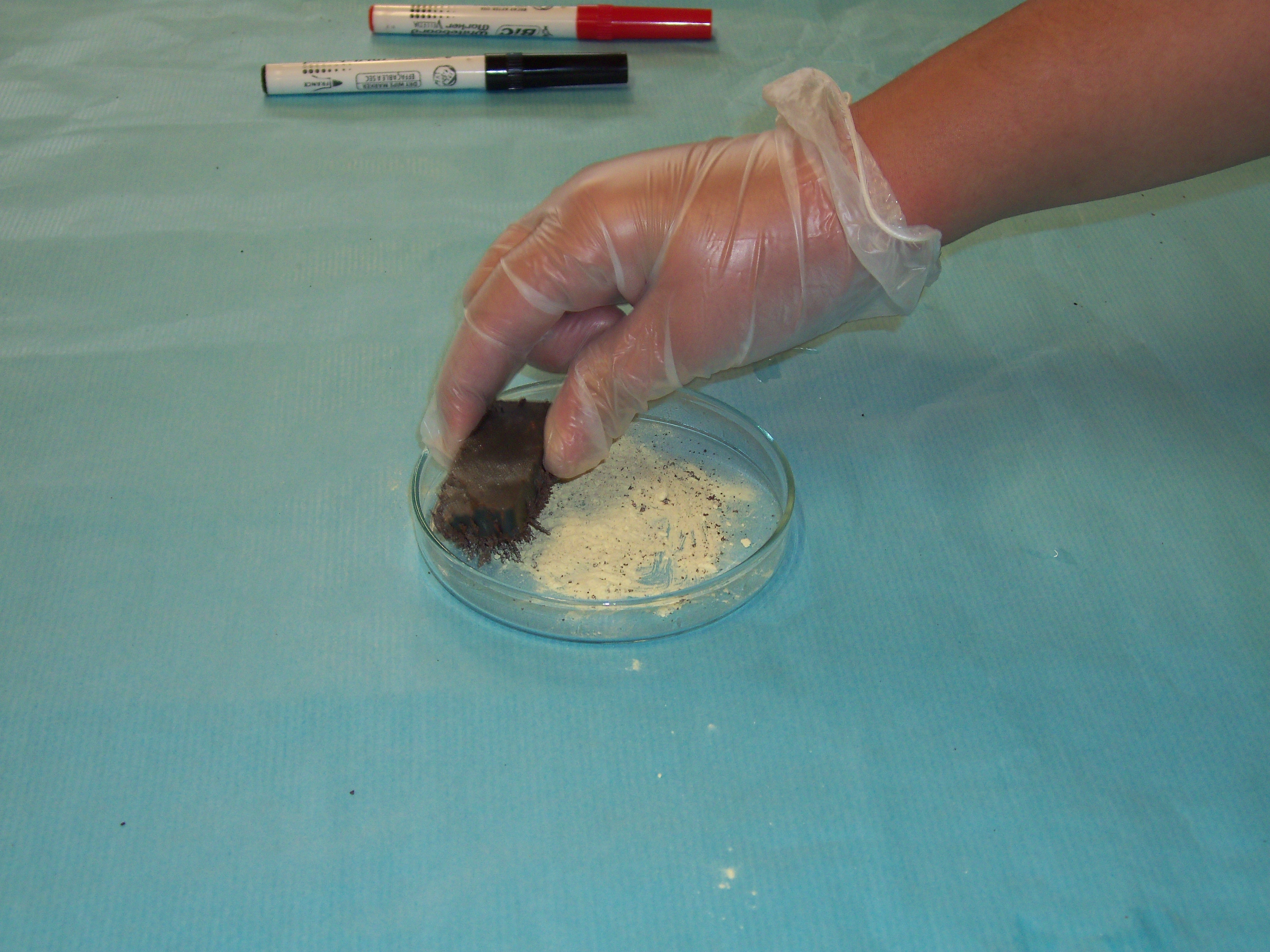
Imagina que tens sobre la taula una barreja de sorra, llimadures de ferro, aigua, sal, oli, alcohol i iode i que el teu objectiu és separar-les en els components inicials.
Abans de continuar llegint pensa com ho faries.
Ep ! Hem dit que no llegiries.
Segurament hagis trobat alguns mètodes possibles. A continuació te’n posem les fotografies.A veure si els identifiques.
Finalment proposa un nom per a cada mètode.
Per deixar-ho clar – TEORIA
Mètodes de separació – REPASSA
Clica aquest enllaç per practicar una mica més sobre els mètodes de separació.
Substàncies pures, mescles i dissolucions – INVESTIGA
Els mètodes que has estudiat abans i que s’utilitzen per a separar substàncies són mètodes físics. Això vol dir que no s’altera la composició de les molècules, ja que no hi ha hagut cap reacció química.
Quan una determinada substància no es pot separar en cap altra de més simple per mètodes físcs diem que és una: (quin nom li posaries ?).
En cas contrari, si una substància, es pot separar en d’altres més simples per mètodes físics diem que es tractarà d’una: (i ara ?).
Finalment d’aquestes darreres n’hi ha de dos tipus. Unes anomenades heterògènies i unes altres d’homogènies.
Finalment et donem algunes substàncies perquè identifiquis de quin tipus dels tres possibles són:
Substància A: Aigua de l’aixeta.
Substància B: Vi.
Substància C: Oli d’oliva verge.
Substància D: Suc de taronja.
Substància E: Tinta de boligraf.
Substància F: Salsa bolognesa.
Les diferències entre substàncies pures, mescles i dissolucions – INVESTIGA
A continuació tens un video molt senzill i instructiu que ens il·lustra sobre les diferències entre substàncies pures i mescles i més endavant entre les mescles homogènies i heterogènies. El mirarem amb atenció i es tracta que en el vostre diari de classe anoteu quines són aquestes diferències. Som-hi !
Solut i disolvent – ANOTA
La major part de substàncis que s’utilitzen al laboratori es troben en forma de dissolució. La majoria de dissolucions estan formades només per dos components. Un dels components s’anomena SOLUT i l’altre DISOLVENT.
El solut és el que es troba en menys quantitat i podríem dir que és el que es DISOL dins de l’altre component. El disolvent en canvi és el que es troba en més quantitat i és el que DISOL al solut dintre seu.
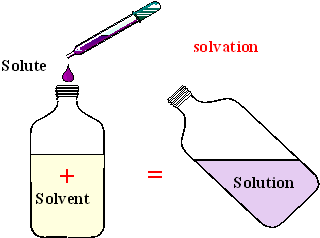 Tant el solut com el disolvent poden estar en diferents estats.
Tant el solut com el disolvent poden estar en diferents estats.
Intenta esbrinar quin és l’estat de cada un dels soluts i disolvents de les següents dissolucions:
AIRE, FANG, CAFÈ AMB LLET, CIMENT, SÈRUM FISIOLÒGIC, ACER
Penseu alguna altra dissolució d’ús comu que hàgiu utilitzat alguna vegada.
Substàncies pures, mescles i dissolucions – Apunts
A continuació trobaràs els apunts corresponent a l’apartat de substàncies pures, mescles i dissolucions que hem treballat fins ara. Et poden ajudar per completar els apunts a la llibreta de teoria i a la vegada per estudiar. Te’n recomanem una lectura detinguda per assegurar-te que has assolit tots els conceptes.


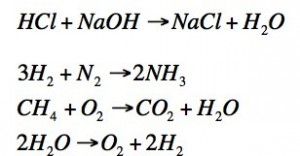


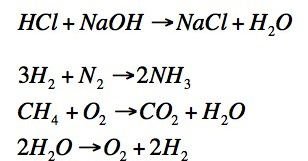





 j
j